Jeśli do roztworu soli włożymy płytkę wykonaną z metalu może zajść reakcja wymiany, która spowoduje zmianę masy tej płytki – zmniejszy się bądź zwiększy się. Reakcja zachodzi wtedy, gdy metal, z którego jest wykonana płytka jest aktywniejszy od metalu znajdującego się w soli, a właściwie w roztworze tej soli 🙂
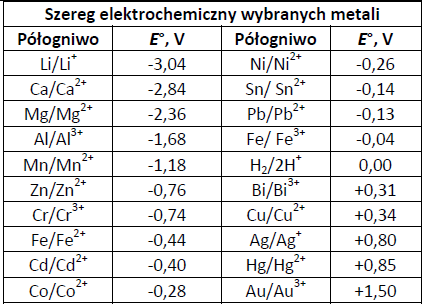
Aktywność metali sprawdzamy w szeregu elektrochemicznym – im niższy potencjał elektrochemiczny E0 tym aktywniejszy metal. Przykładowo chrom jest bardziej aktywny od miedzi, a miedź jest bardziej aktywna od srebra.
Zadania maturalne z płytek można podzielić na dwa typy:
- Mamy podaną zmianę masy płytki po zajściu reakcji
- Mamy podany ubytek masy płytki po zajściu reakcji oraz oczyszczeniu jej z osadzonego na niej metalu
W tej lekcji rozpracujemy te dwa typy zadań. Zapraszam 🙂
Subskrybuj nasz kurs online, aby uzyskać dostęp do pełnej treści lekcji.
Jeśli jeszcze nie potrzebujesz subskrypcji, sprawdź koniecznie nasze przykładowe lekcje dostępne zupełnie za darmo!


