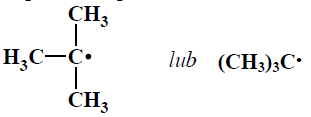Energia dysocjacji wiązania
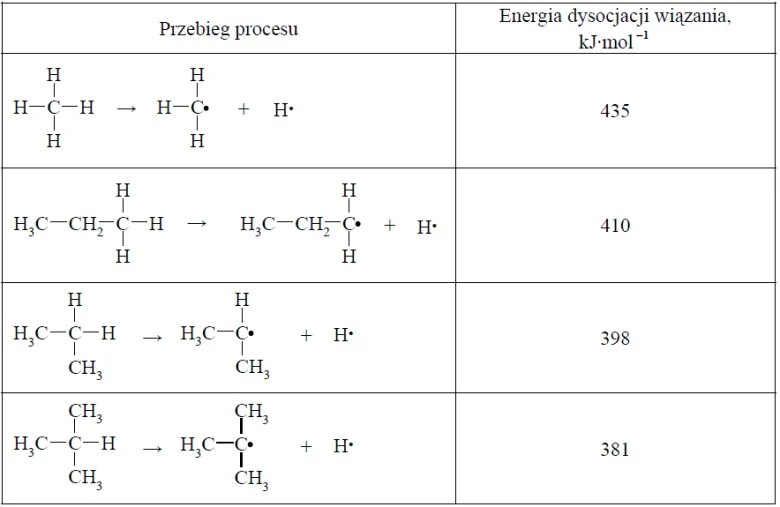
Energia dysocjacji wiązania C–H w alkanach (wyrażona w kJ·mol –1 ) to energia, jaką trzeba dostarczyć, aby przekształcić 1 mol alkanu w 1 mol atomów wodoru i 1 mol odpowiedniego rodnika organicznego.
Przykłady takich procesów oraz odpowiadające im energie dysocjacji zestawiono w poniższej tabeli.
Można zauważyć, że łatwość odrywania atomu wodoru od cząsteczki alkanu zależy od rzędowości atomu węgla, z którym jest on połączony.
a) Korzystając z informacji, podkreśl przybliżoną wartość energii dysocjacji wiązania C–H w etanie.
435 kJ·mol –1 410 kJ·mol –1 398 kJ·mol –1 381 kJ·mol –1
b) Spośród rodników, których wzory podano w informacji, wybierz i napisz wzór tego, który tworzy się najłatwiej.
.......................................................................................................................................................
Załóż bezpłatne konto, aby uzyskać dostęp do rozwiązania tego zadania.