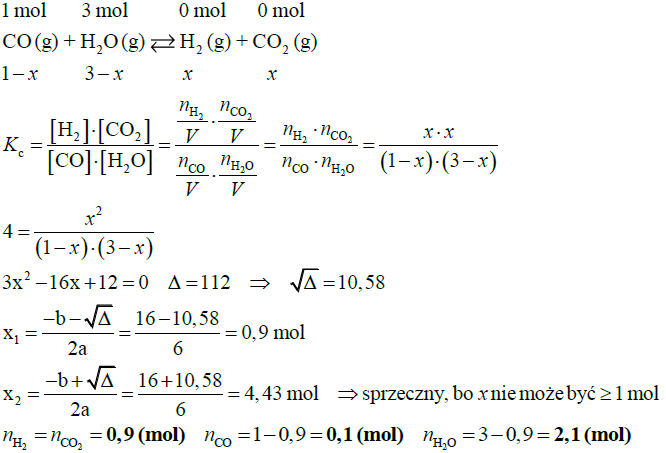Obliczanie liczby moli każdej substancji znajdującej się w reaktorze po ustaleniu się stanu równowagi
Reakcja tlenku węgla(II) z parą wodną przebiega zgodnie z równaniem:
CO(g) + H2O(g) ↔ H2(g) + CO2(g)
W temperaturze 800 K stężeniowa stała równowagi tej reakcji jest równa 4,0.
W zamkniętym reaktorze o stałej pojemności zmieszano 1 mol tlenku węgla(II) z parą wodną w ilości trzykrotnie większej od ilości stechiometrycznej. Mieszaninę utrzymywano w temperaturze 800 K aż do osiągnięcia stanu równowagi dynamicznej przez układ.
Oblicz liczbę moli każdej substancji znajdującej się w reaktorze po ustaleniu się stanu równowagi opisanej reakcji.
Obliczenia:
Załóż bezpłatne konto, aby uzyskać dostęp do rozwiązania tego zadania.