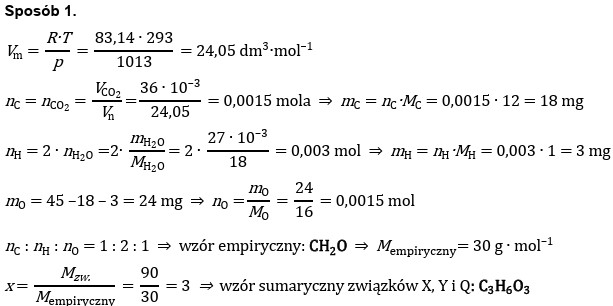Zadanie 25, arkusz maj 2024
Trzy związki organiczne X, Y i Q są izomerami o masie molowej równej 90 g ∙ mol–1. W wyniku spalenia 45 mg jednego z tych związków otrzymano 27 mg wody oraz 36,0 cm3 tlenku węgla(IV) odmierzonego w temperaturze 293 K i pod ciśnieniem 1013 hPa.
O cząsteczkach tych związków wiadomo, że:
• szkielet każdej z cząsteczek stanowią połączone atomy węgla
• cząsteczki związków X i Y są chiralne, a związku Q – achiralne
• cząsteczki związków Y i Q mają takie same grupy funkcyjne
• odczyn wodnego roztworu związku X jest obojętny, a odczyn wodnego roztworu związku Y – kwasowy.
Przeprowadzono następujące doświadczenie: do próbki związku X wprowadzono zawiesinę świeżo strąconego Cu(OH)2, wymieszano (na zimno), a następnie ogrzano. Wyniki tego eksperymentu zilustrowano na poniższych zdjęciach.

Na podstawie obliczeń ustal wzór elementarny i rzeczywisty (sumaryczny) opisanych związków.
Następnie napisz:
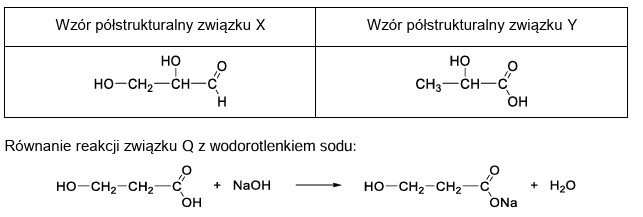
• wzory półstrukturalne (grupowe) związków X i Y
• w formie cząsteczkowej równanie reakcji związku Q z wodorotlenkiem sodu.
Zastosuj wzory półstrukturalne (grupowe) związków organicznych. Uniwersalna stała gazowa 𝑹 = 𝟖𝟑,𝟏𝟒 𝐡𝐏𝐚∙𝐝𝐦𝟑 ∙𝐦𝐨𝐥 –𝟏 ∙𝐊–𝟏.
Obliczenia:
Równanie reakcji związku Q z wodorotlenkiem sodu:
……………………………………………………………………………………………………………………………….
Załóż bezpłatne konto, aby uzyskać dostęp do rozwiązania tego zadania.