Defekt masy i stabilność jąder
W jądrze atomowym istnieją siły jądrowe między nukleonami, które działają na małą odległość i nie są zależne od ładunku. Przy zderzeniach neutronów z protonami może dojść do wymiany ładunku, czyli zamiany protonu w neutron i odwrotnie. Energię odziaływań pomiędzy nukleonami można wyliczyć. Przykładowo masa atomowa helu powinna być równa sumie mas dwóch protonów i dwóch neutronów tj. 4,0319 u.
masa 2 protonów 2*1,0072766 u = 2,0145532 u
masa 2 neutronów 2*1,0086654 u =2,0173308 u
w sumie 4,0318840 u
Jednak najdokładniejsze eksperymentalne oznaczenia masy atomowej helu dają wartość 4,0015 u. Różnica 0,03039 nosi nazwę defektu (niedoboru) masy. Stosując równanie Einsteina E=mc
Źródło: Chemia. Od A do Z. Repetytorium, M. Klimaszewska, Warszawa 1998
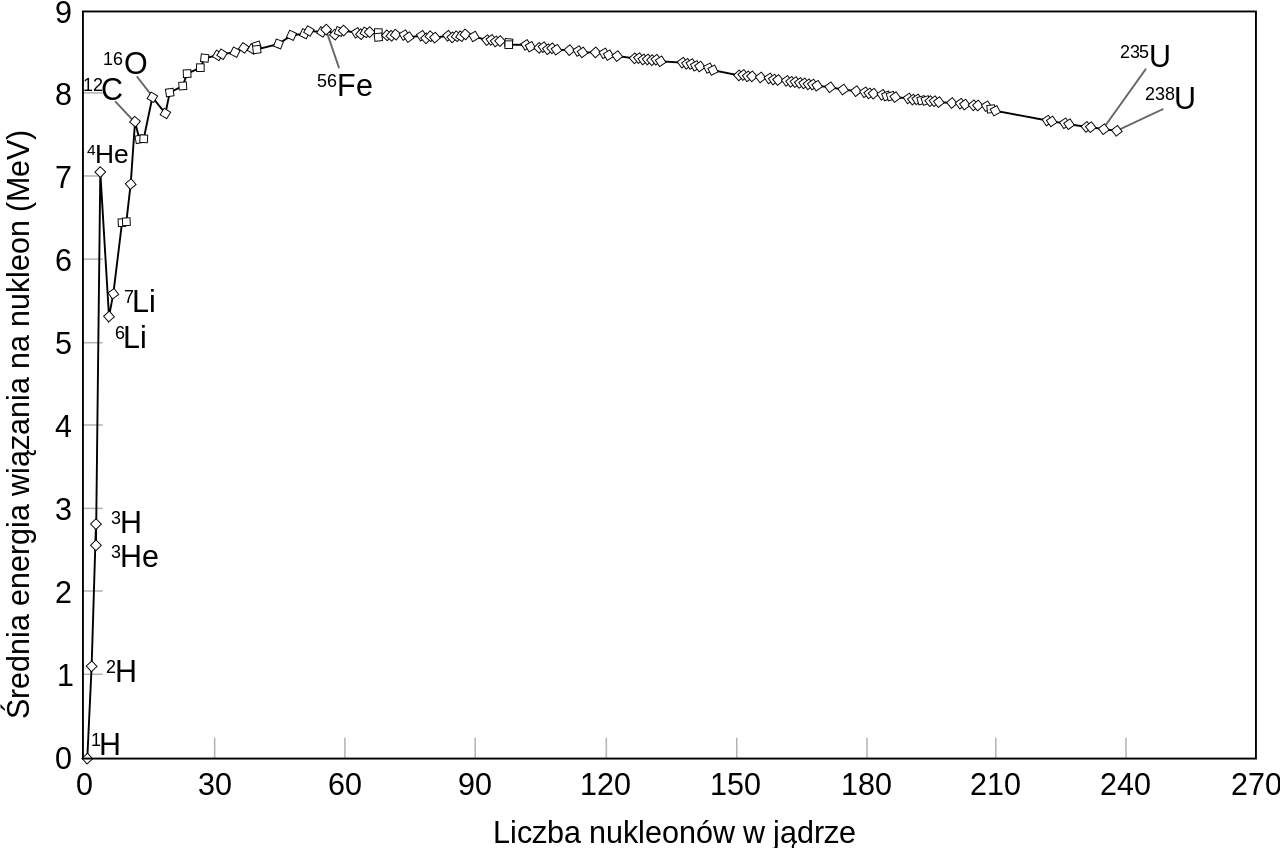
a) Przeanalizuj poniższy wykres i podkreśl właściwie wyrażenia tak, aby powstały zdania prawdziwe.
Wykres średniej energii wiązania na nukleon od liczby nukleonów w jądrze jest krzywą, która szybko narasta dla (dużych/małych) liczb masowych, a stopniowo opada dla (dużych/małych). Na tej podstawie można wywnioskować, że dla pierwiastków lekkich syntezie nukleonów jąder towarzyszy (uwalnianie/pobieranie) energii, natomiast w przypadku pierwiastków ciężkich (uwalnianie/pobieranie) energii towarzyszy rozszczepianiu, czyli podziałowi jąder. Z tego również powodu jądra pierwiastków lekkich charakteryzują się (małą/dużą) trwałością.
b) Z jakiego powodu izotop 56Fe jest pierwiastkiem występującym w dużej ilości w przyrodzie?
Subskrybuj nasz kurs chemii online, aby uzyskać dostęp do tego i wielu innych zadań z rozwiązaniami!
a) Wykres średniej energii wiązania na nukleon od liczby nukleonów w jądrze jest krzywą, która szybko narasta dla (dużych/małych) liczb masowych, a stopniowo opada dla (dużych/małych). Na tej podstawie można wywnioskować, że dla pierwiastków lekkich syntezie nukleonów jąder towarzyszy (uwalnianie/pobieranie) energii, natomiast w przypadku pierwiastków ciężkich (uwalnianie/pobieranie) energii towarzyszy rozszczepianiu, czyli podziałowi jąder. Z tego również powodu jądra pierwiastków lekkich charakteryzują się (małą/dużą) trwałością.
b) Z wykresu wynika, że izotop 56Fe ma największą energię wiązania na nukleon, co świadczy o jego dużej stabilności. Wynika to z faktu, że izotop ten ma w przybliżeniu taką samą liczbę protonów (26) i neutronów (30). Ponadto obie te liczby są parzyste.
Subskrybuj nasz kurs chemii online, aby uzyskać dostęp do tego i wielu innych zadań z rozwiązaniami!