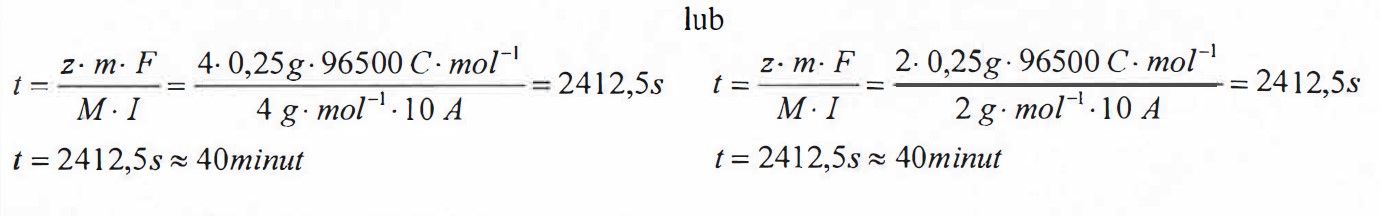Elektroliza wodnego roztworu NaOH – czas elektrolizy
W procesie elektrolizy wodnego roztworu wodorotlenku sodu na elektrodach platynowych zachodzą następujące procesy na katodzie i anodzie:
K(−): 4H2O + 4e-→ 2H2 + 4OH-
A(+): 2H2O → O2 + 4H+ + 4e-
Oblicz, ile minut należy prowadzić elektrolizę wodnego roztworu wodorotlenku sodu prądem o natężeniu 10 A, aby otrzymać 2,8 dm3 wodoru w warunkach normalnych.
Przyjmij następujące założenia:
- wydajność prądowa procesu elektrolizy wynosi 100%
- wartość stałej Faradaya F = 96500 C/mol
Wynik podaj w zaokrągleniu do liczby całkowitej.
| Obliczenia:
Odpowiedź: . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . |
Subskrybuj nasz kurs chemii online, aby uzyskać dostęp do tego i wielu innych zadań z rozwiązaniami!