Reakcje egzo i endotermiczne
W czystej wodzie ustala się stan równowagi reakcji autoprotolizy, która zachodzi zgodnie z równaniem:
2H2O ⇄ H3O+ + OH-
Tę reakcję opisuje stała równowagi nazywana iloczynem jonowym wody. Wyraża się ona równaniem:
Kw=[H3O+]∙[OH-]
Poniżej przedstawiono wartości iloczynu jonowego wody Kw w zakresie temperatury 0 ºC –100 ºC (pod ciśnieniem atmosferycznym).
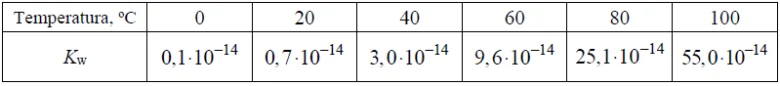
Uzupełnij poniższe zdania. Wybierz i zaznacz jedno określenie spośród podanych w każdym nawiasie.
Reakcja autodysocjacji wody jest (egzoenergetyczna / endoenergetyczna). Wraz ze wzrostem temperatury pH czystej wody (maleje / rośnie / nie ulega zmianie).
Reakcja autodysocjacji wody jest (egzoenergetyczna / endoenergetyczna). Wraz ze wzrostem temperatury pH czystej wody (maleje / rośnie / nie ulega zmianie).
Załóż bezpłatne konto, aby uzyskać dostęp do rozwiązania tego zadania.


