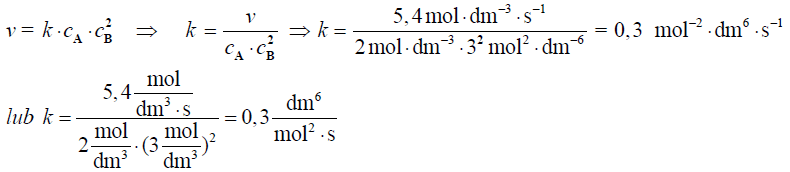Równanie kinetyczne i szybkość reakcji
Reakcja A + 2B ⇄ C przebiega w temperaturze T według równania kinetycznego v = k·cA·cB2. Początkowe stężenie substancji A było równe 2 mol · dm−3 , a substancji B było równe 3 mol·dm−3 . Szybkość początkowa tej reakcji była równa 5,4 mol · dm−3 · s −1 .
a) Oblicz stałą szybkości reakcji w temperaturze T, wiedząc, że dla reakcji przebiegającej według równania kinetycznego v = k·cA·cB2 stała szybkości k ma jednostkę: mol −2 · dm6 · s −1.
Obliczenia:
Odpowiedź:
b) Korzystając z powyższych informacji, oblicz szybkość reakcji w momencie, gdy przereaguje 60% substancji A. Wynik podaj z dokładnością do czwartego miejsca po przecinku.
Obliczenia:
Odpowiedź:
Załóż bezpłatne konto, aby uzyskać dostęp do rozwiązania tego zadania.