Wiązania sigma i pi oraz kształt cząsteczek
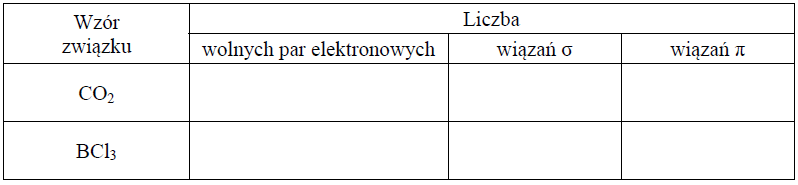
a) Uzupełnij poniższą tabelę − wpisz liczbę wolnych par elektronowych oraz liczbę wiązań σ i π w cząsteczkach CO2 i BCl3.
 b) Określ kształt (liniowy, tetraedryczny, trójkątny) cząsteczek obu związków.
b) Określ kształt (liniowy, tetraedryczny, trójkątny) cząsteczek obu związków.
Kształt cząsteczki CO2: ................................................................................................................
Kształt cząsteczki BCl3: ...............................................................................................................
a)
CO2 :
liczba wolnych par elektronowych: 4
wiązań sigma: 2
wiązań pi: 2
BCl3 :
liczba wolnych par elektronowych: 9
wiązań sigma: 3
wiązań pi: 0
Kształt cząsteczki CO2: liniowy
Kształt cząsteczki BCl3: trójkątny
Załóż bezpłatne konto, aby uzyskać dostęp do rozwiązania tego zadania.


