Zadanie 13, arkusz maj 2022
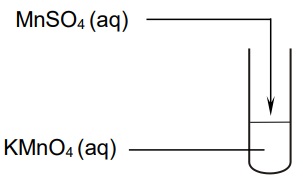
Wykonano doświadczenie zilustrowane poniższym schematem.
Po zakończeniu reakcji w probówce widoczne były bezbarwny roztwór i brunatny osad.
Napisz w formie jonowej skróconej, z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy), równania procesów redukcji i utleniania zachodzących podczas opisanej przemiany. Uwzględnij, że reakcja zachodzi w środowisku obojętnym.
Równanie procesu redukcji:
.................................................................................................................................................
Równanie procesu utleniania:
.................................................................................................................................................
Równanie procesu redukcji:
MnO4−+ 2H2O + 3e− → MnO2 + 4OH− (x 2)
ALBO
MnO4−+ 4H++ 3e− → MnO2 + 2H2O ALBO MnO4−+ 4H3O++ 3e− → MnO2 + 6H2O (x 2)
Równanie procesu utleniania:
Mn2++ 2H2O → MnO2 + 4H++ 2e− ALBO Mn2++ 6H2O → MnO2 + 4H3O++ 2e− (x 3)
ALBO
Mn2++ 4OH− → MnO2 + 2H2O + 2e− (x 3)
Załóż bezpłatne konto, aby uzyskać dostęp do rozwiązania tego zadania.