Zadanie 21.1, arkusz maj 2024
Przygotowano próbki czterech kwasów:
• CH3COOH
• CH2ClCOOH
• CHCl2COOH
• CCl3COOH
Wszystkie roztwory miały jednakową objętość. Stężenie molowe każdego kwasu było równe 1 mol ∙ dm–3. Do roztworów tych kwasów, znajdujących się w probówkach w przypadkowej kolejności, dodano po pięć kropli roztworu fioletu metylowego, który jest wskaźnikiem pH. Wyniki doświadczenia przedstawiono na zdjęciach.

Fragment skali barw dla fioletu metylowego w roztworach o różnym pH przedstawia poniższy rysunek.
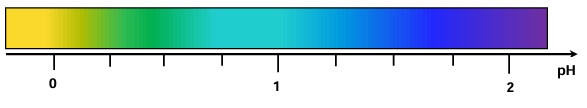
Wartości p𝐾a dla kwasów użytych w doświadczeniu, podane w przypadkowej kolejności, wynoszą: 2,87; 4,76; 0,66; 1,35.
Na podstawie informacji wstępnej wybierz probówkę, w której znajduje się roztwór najmocniejszego kwasu, i dokończ zdania.
Roztwór najmocniejszego kwasu znajduje się w probówce oznaczonej literą ……… .
Wzór tego kwasu to: ……………….……………….……………. . [wzór półstrukturalny (grupowy)]
Wyjaśnij, dlaczego wybrany kwas wykazuje największą moc. W wyjaśnieniu odwołaj się do budowy cząsteczek tego związku.
Wyjaśnienie: ..…………………………………………………………………………………………..
Roztwór najmocniejszego kwasu znajduje się w probówce oznaczonej literą B. Wzór tego kwasu to: CCl3COOH. Wyjaśnienie: Obecność (trzech) atomów chloru (o dużej elektroujemności) w cząsteczce kwasu w sąsiedztwie grupy karboksylowej ((powoduje wzmocnienie efektu indukcyjnego), najbardziej ułatwia oderwanie kationu wodoru od grupy karboksylowej, dzięki czemu moc kwasu rośnie (albo jest większa od kwasu CH3COOH)).
Załóż bezpłatne konto, aby uzyskać dostęp do rozwiązania tego zadania.


