Wodorosole, teorie kwasów i zasad, hydroliza
Przeprowadzono doświadczenie zilustrowane poniższym schematem.
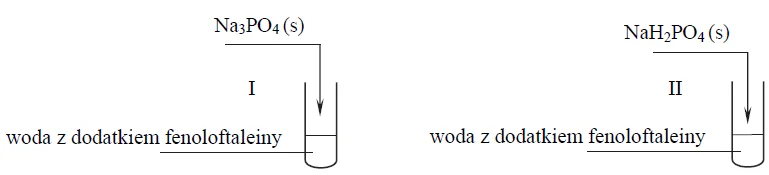 Powstanie malinowego zabarwienia roztworu zaobserwowano tylko w jednej probówce, a pH wodnego roztworu w probówce, w której nie uzyskano malinowego roztworu, było mniejsze od 7.
Powstanie malinowego zabarwienia roztworu zaobserwowano tylko w jednej probówce, a pH wodnego roztworu w probówce, w której nie uzyskano malinowego roztworu, było mniejsze od 7.
Z dwóch jonów : PO43- i H2PO4- tylko jeden może pełnić zarówno funkcję zasady jak i kwasu Bronsteda.
Wybierz ten jon. Uzupełnij podane poniżej zapisy, tak aby otrzymać dwa równania reakcji (w środowisku kwasowym i zasadowym) z udziałem wybranego jonu.
............................... + H3O+ → ............................... + ...............................
............................... + OH− → ............................... + ...............................
H2PO4– + H3O+ → H3PO4 + H2O
H2PO4– + OH– → HPO42- + H2O
Załóż bezpłatne konto, aby uzyskać dostęp do rozwiązania tego zadania.


