Charakter chemiczny to nie to samo, co odczyn!
Wielu uczniów używa zamiennie pojęć charakter chemiczny i odczyn. Jednak oznaczają one coś zupełnie innego i nie można ich traktować jak synonimy. Przeanalizujmy w takim razie w czym tkwi różnica i jak prawidłowo tych pojęć należy używać.
Charakter chemiczny
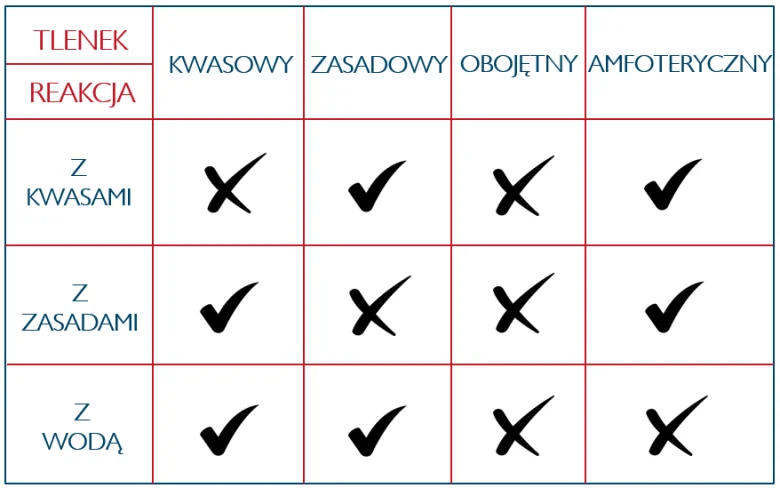
Charakter chemiczny określa w jaki sposób dana substancja zachowuje się w stosunku do kwasów, wodorotlenków i wody.
Wyróżniamy cztery charaktery chemiczne:
- kwasowy
- zasadowy
- obojętny
- amfoteryczny
Charakter chemiczny określamy najczęściej dla tlenków i wodorków. Poniżej tabelka dla tlenków.
Odczyn
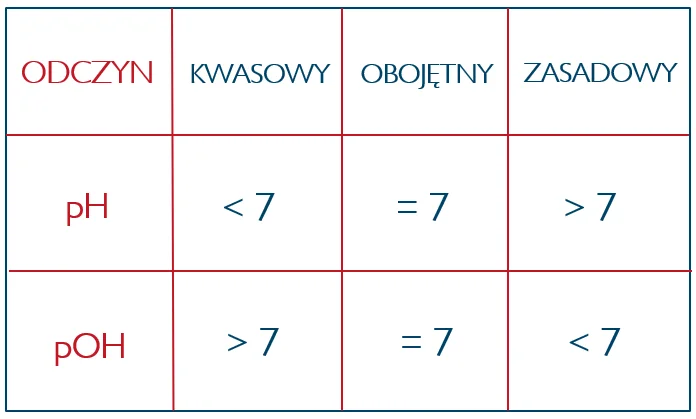
Odczyn mówi nam o pH lub pOH roztworu danej substancji chemicznej.
Nie można powiedzieć, że np. wodorotlenek sodu ma odczyn zasadowy. Ten związek jest substancją stałą, a odczyn określamy dla wodnych roztworów substancji chemicznych. W związku z tym to roztwór NaOH ma odczyn zasadowy.
Wyróżniamy trzy rodzaje odczynów:
- kwasowy
- zasadowy
- obojętny
Odczyn zależy od stężenia jonów H+ i jonów OH– w roztworze wodnym danej substancji.
Im więcej jest w nim jonów H+ , tym bardziej kwasowy odczyn ma roztwór, a tym samym niższe pH i wyższe pOH.
Im więcej jest w nim jonów OH– , tym bardziej zasadowy odczyn ma roztwór, a tym samym wyższe pH i niższe pOH.
Jeśli stężenie jonów H+ i OH– w roztworze jest takie samo, to odczyn takiego roztworu jest obojętny, a pH i pOH jest równe 7.
Poniższe zestawienie powinno rozwiać wszelkie wątpliwości.
Przykład 1
SiO2
Charakter chemiczny: kwasowy
Dowód: SiO2 + 2NaOH ➞ Na2SiO3 + H2O
Odczyn wodnego roztworu: obojętny (a właściwie odczyn wody, ponieważ SiO2 w wodzie się praktycznie nie rozpuszcza, więc ciężko mówić o wodnym roztworze SiO2).
Dowód: SiO2 jest głównym składnikiem piasku, nie reaguje z wodą. W innym wypadku nie byłoby plaż.
P.S. Pamiętaj, że tlenek kwasowy nie musi być kwasotwórczy! “Kwasotwórczy” oznacza, że w reakcji z wodą tworzy kwas tlenowy. Natomiast “kwasowy” oznacza, że reaguje z substancjami o charakterze zasadowym. Tlenek krzemu (IV) jest zatem jest kwasowy, ale nie jest kwasotwórczy.
Przykład 2
N2O5
Charakter chemiczny: kwasowy
Dowód: N2O5 + 2KOH ➞ 2KNO3 + H2O
Odczyn wodnego roztworu: kwasowy
(a właściwie odczyn roztworu produktu jego reakcji z wodą)
Dowód: N2O5 + H2O ➞ 2HNO3
HNO3 ➞ H+ + NO3–
Przykład 3
Al2O3
Charakter chemiczny: amfoteryczny
Dowód: Al2O3 + 6HCl ➞ 2AlCl3 + 3H2O
Al2O3 + 2KOH + 3H2O ➞ 2K[Al(OH)4]
Odczyn wodnego roztworu: obojętny
Al2O3 nie reaguje z wodą
Przykład 4
NO
Charakter chemiczny: obojętny
Dowód: NO nie reaguje z kwasami, zasadami, wodą
Odczyn wodnego roztworu: obojętny
Dowód: NO nie reaguje z wodą (chyba, że go zmusimy i użyjemy odpowiednich warunków tj. temperatura, katalizator itd., jednak bez “dodatków” reakcja nie zachodzi)
Mam nadzieję, że ten wpis rozwiał wątpliwości w jakich sytuacjach określamy odczyn roztworu, a w jakich charakter chemiczny substancji. Jeśli masz pytania, zostaw je w komentarzu.