Konfiguracja elektronowa – zasady
- Żaden orbital nie może być obsadzony przez więcej niż dwa elektrony, gdy zaś dwa elektrony zajmują jeden orbital, ich spiny muszą być sparowane.
- Elektrony w atomie obsadzają najpierw orbitale o najniższej energii, a dopiero potem orbitale o wyższej energii.
- Atom w stanie podstawowym przyjmuje konfigurację o największej liczbie elektronów niesparowanych. .Elektrony zajmują orbitale danej podpowłoki pojedynczo, zanim obsadzą którykolwiek z nich podwójnie.
Źródło: Podstawy chemii fizycznej, Peter William Atkins, Warszawa 2002
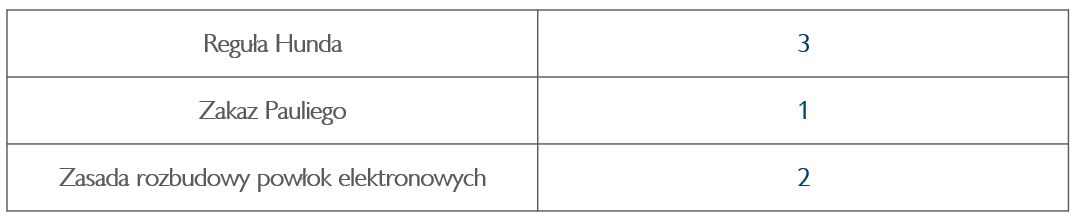
Dopasuj numer zdania do odpowiedniej reguły:
Subskrybuj nasz kurs chemii online, aby uzyskać dostęp do tego i wielu innych zadań z rozwiązaniami!
Subskrybuj nasz kurs chemii online, aby uzyskać dostęp do tego i wielu innych zadań z rozwiązaniami!