Aktywność metali
Cyna nie ulega działaniu słabych kwasów i zasad, dzięki czemu jest stosowana do pokrywania blachy stalowej w celu jej ochrony przed korozją. Z blachy tej wykonuje się puszki na konserwy. Aby odzyskać cyn z odpadów, działa się na nią chlorem i przekształca w chlorek cyny(IV). Mocne kwasy i zasady atakują cynę energicznie. W reakcji ze stężonym kwasem solnym cyna tworzy chlorek cyny(II), który jest solą dobrze rozpuszczalną w wodzie.
Szereg aktywności metali tworzą metale i wodór ułożone według ich podatności na utlenianie, czyli według zdolności tworzenia jonów naładowanych dodatnio. Każdy pierwiastek jest reduktorem kationów wszystkich pierwiastków położonych po jego prawej stronie w tym szeregu. Poniżej przedstawiono fragment szeregu aktywności metali.
Zn/Zn2+ Sn/Sn2+ H2/H+ Cu/Cu2+
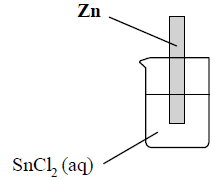
a) Wskaż metal (cynk Zn albo miedź Cu), z którego wykonaną blaszkę należy zanurzyć w wodnym roztworze chlorku cyny(II), aby wydzieliła się cyna metaliczna. Uzupełnij schemat doświadczenia, wpisując symbol wybranego metalu
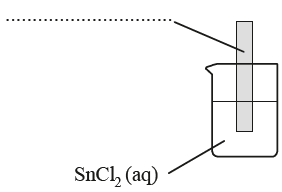 b) Napisz w formie jonowej równanie reakcji chemicznej, która zachodzi w czasie doświadczenia.
b) Napisz w formie jonowej równanie reakcji chemicznej, która zachodzi w czasie doświadczenia.
......................................................................................................................................................
Załóż bezpłatne konto, aby uzyskać dostęp do rozwiązania tego zadania.